
Thuốc viên điều trị nhiễm trùng đường ruột tái phát chiết xuất từ phân người
TNNN - Một loại thuốc viên chứa bào tử vi khuẩn được phân lập từ phân người có thể sẽ trở thành thuốc uống điều trị nhiễm trùng đường ruột tái phát đầu tiên được chấp thuận.
Nhiễm trùng đường ruột do vi khuẩn Clostridium difficile đặc biệt nguy hiểm ở những người có hệ vi khuẩn đường ruột không khỏe mạnh, chẳng hạn như người già hoặc sử dụng kháng sinh dài hạn. Phương pháp điều trị hiện nay là cấy ghép hệ vi sinh vật trong phân (FMT): phân từ một người hiến tặng khỏe mạnh, đưa vào bệnh nhân qua đường nội soi, giúp khôi phục sự cân bằng của hệ vi khuẩn đường ruột và ngăn nhiễm khuẩn Clostridium difficile. Tuy nhiên, đây là một liệu pháp xâm lấn, chưa kể vật liệu cấy ghép rất khó để tiêu chuẩn hóa, theo Sahil Khanna, bác sĩ tiêu hóa tại Mayo Clinic, người tham gia vào các thử nghiệm SER-109 trước đây.
Đã có trường hợp phân của người hiến tặng truyền bệnh nhiễm trùng mới có hại cho bệnh nhân. Năm 2019, một bệnh nhân nam có hệ miễn dịch bị tổn hại đã tử vong sau khi nhận phân có chứa vi khuẩn Escherichia coli kháng kháng sinh. COVID-19 cũng làm tăng mối lo về an toàn: FMT có thể làm lây nhiễm SARS-CoV-2.
Do đó, năm 2020, Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đưa ra nhiều yêu cầu sàng lọc khắt khe hơn đối với quy trình FMT. Điều này khiến cho việc sàng lọc người hiến tặng trở nên càng khó khăn, trong khi các nguồn chế phẩm cần thiết để xử lý phân đang cạn kiệt. Nhà cung cấp lớn nhất của Mỹ, ngân hàng phân phi lợi nhuận OpenBiome, cho biết đã ngừng sản xuất từ tháng 2/2021do gặp khó khăn về tài chính và các lựa chọn thay thế FMT sắp xuất hiện.
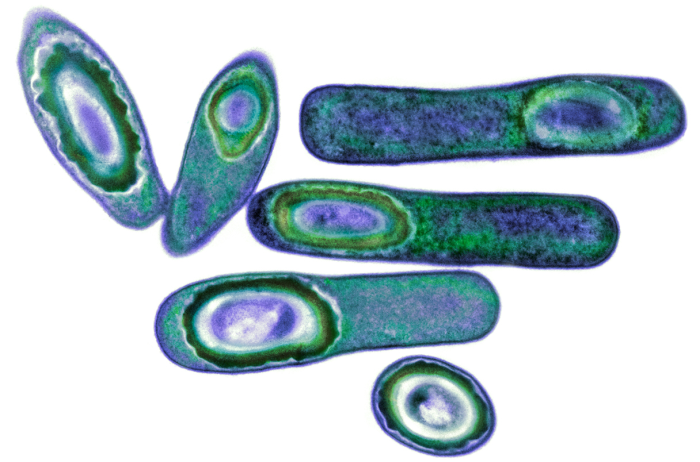
Vi khuẩn Clostridium difficile, có thể gây chết người nếu liên tục tái nhiễm.
Một trong số đó là thuốc SER-109 của công ty Seres Therapeutics đã thành công trong thử nghiệm giai đoạn 3. Phân từ những người hiến tặng được sàng lọc, rồi xử lý bằng ethanol để loại bỏ các virus, nấm và vi khuẩn “sinh dưỡng” - những vi khuẩn đang trong tình trạng phát triển và sinh sản. Quy trình xử lý chỉ để lại những vi khuẩn có thể hình thành những cấu trúc có thành dày, gọi là bào tử, phần lớn thuộc nhóm Firmicutes.
Các vi khuẩn thuộc nhóm này có giá trị vì chúng có thể cạnh tranh với C. difficile trong ruột. Giám đốc Y tế Lisa von Moltke của Seres, cho biết: “lấy không gian và thức ăn cũng như nguồn carbon của C. difficile”. Firmicute cũng thay đổi thành phần của axit mật trong ruột, làm cho môi trường ruột trở nên ít thích hợp hơn đối với C. difficile.
Năm 2016, Seres đã phải tuyên bố phương pháp điều trị của họ không cho thấy lợi ích lớn hơn so với giả dược trong thử nghiệm giai đoạn 2. Tuy nhiên, các nhà nghiên cứu của công ty sau đó kết luận rằng liều lượng thử nghiệm quá thấp, chưa tuyển chọn đúng những người tham gia thực sự bị nhiễm trùng tái phát. Thử nghiệm giai đoạn 3 của Seres, sử dụng liều cao hơn và xét nghiệm sàng lọc chính xác hơn, bao gồm 182 người bị nhiễm C. difficile tái phát.
Những người này được chia ngẫu nhiên vào hai nhóm: nhận SER-109 hoặc giả dược; cả hai nhóm đều trải qua một đợt sử dụng kháng sinh. Kết quả, tỷ lệ nhiễm C. difficile tái phát ở nhóm dùng giả dược là 40%và ở nhóm uống SER-109 là 12%, theo nhóm nghiên cứu báo cáo trên Tạp chí Y học New England.
Kết quả này tương đương với điều trị bằng FMT, theo Colleen Kelly, nhà tiêu hóa học tại trường Đại học Brown, người từng thực hiện một thử nghiệm SER-109 trước đây nhưng không tham gia thử nghiệm mới. Đáng lưu ý, nhiều bệnh nhân muốn tránh cảm giác khó chịu khi nội soi và sẽ chọn thuốc viên nếu có.
Các nhà nghiên cứu khác nghi ngờ liệu pháp mới chưa thể đạt hiệu quả như FMT. Alexander Khoruts, nhà tiêu hóa tại trường Đại học Minnesota, cho biết: “Hệ sinh vật hoàn chỉnh trong phân là một tiêu chuẩn thực sự cao mà thiên nhiên đã thiết lập". Khoruts lưu ý rằng quá trình thanh lọc để điều chế SER-109 đã loại bỏ cả các virus tiêu diệt vi khuẩn được gọi là phage.
Khoruts nói: “Chỉ cung cấp khuẩn Firmicutes vẫn tốt hơn giả dược, nhưng tôi cho rằng không thể bỏ qua các thành phần vi khuẩn khác trong phân" .
Seres đặt mục tiêu nộp đơn xin FDA chấp thuận SER-109 vào giữa năm 2022. Một số đối thủ cạnh tranh cũng đang theo sát gót. Năm ngoái, công ty Rebiotix Inc. đã công bố kết quả khả quan từ thử nghiệm giai đoạn 3 về phương pháp điều trị C. difficile tái phát - thuốc của Rebiotix Inc. là một sản phẩm phân đã lọc đưa vào cơ thể theo đường thụt hậu môn.
Tháng 10/2021, Finch Therapeutics, một nhánh của OpenBiome, tuyên bố đã thử nghiệm thành công giai đoạn 2 thuốc viên chứa phân đông khô. Công ty Vedanta Biosciences đã hoàn thành thử nghiệm giai đoạn 2 của một liệu pháp điều trị C. difficile tái phát, bao gồm tám chủng vi khuẩn được chọn lọc riêng lẻ, nuôi trong ngân hàng tế bào chứ không phải phân lập từ phân.
Với các lựa chọn thay thế FMT, "tôi không muốn phải chứng kiến mô hình ngân hàng phân biến mất hoàn toàn”, Kelly nói, lưu ý rằng phân vẫn sẽ rất quan trọng đối với việc nghiên cứu các bệnh khác như bệnh viêm ruột. Nhưng ông rất háo hức về việc triển khai SER-109 cho bệnh nhân C. difficile. Kelly nói: “Tôi nghĩ mọi người đều rất vui khi có thứ một phương pháp điều trị an toàn, ổn định và sẵn có.Chỉ hy vọng nó không quá đắt”.
Nguồn: Khoa học & Phát triển
Bình luận
Tin khác


Gợi mở về vai trò của diêm tiêu Việt Nam trong lịch sử thế giới

Thiết kế pin mới giúp giảm nguy cơ cháy nổ

JASIS 2025 – Triển lãm thiết bị khoa học và phân tích hàng đầu châu Á

Cấp thiết sửa đổi quy chuẩn kỹ thuật quốc gia cho sản phẩm sữa chế biến

Kiểm tra, xác nhận giá trị sử dụng phương pháp; ước lượng độ không đảm bảo đo lĩnh vực sinh học
Tin cũ hơn

Đảm bảo chất lượng kết quả thử nghiệm

Nhận thức chung ISO/IEC 17025:2017 và đánh giá nội bộ

Xác nhận giá trị sử dụng phương pháp thử trong phân tích hóa học

Triệt để tránh tình trạng “dễ làm, khó bỏ” trong nghiên cứu khoa học

Báo động: Vi nhựa xâm nhập não người với tốc độ nhanh













